Comment l'acier se Corrode?
- 16 mai 2022
- 6 min de lecture
La corrosion est la détérioration du métal par un processus électrochimique. La corrosion est présente chaque fois qu'il y a deux métaux ou acier différents dans la même structure, un électrolyte ou de l'eau avec n'importe quel type de sels dissous et un chemin conducteur entre les métaux différents.

Lorsque des particules de fer ont été exposées à l'oxygène et à l'humidité, la rouille commence à se former.

Les particules de fer sont ensuite oxydées, formant Fe2+. Lorsque Fe2+ est formé, 4e- sont libérés et les électrons libres sont transférés vers des sites moins actifs, puis l'oxygène est converti en ion oxygène.
La recombinaison de ces ions produit un hydroxyde ferreux produit de corrosion du fer.

Cette réaction est communément appelée flux de courant de l'anode (site plus actif) à la cathode. (site moins actif).
Toute structure métallique exposée à l'environnement se corrodera avec le temps. Le taux de corrosion dépend de l'environnement dans lequel se trouve le métal. Étant donné que la corrosion atmosphérique est si répandue, il est recommandé de prendre des mesures de précaution efficaces en matière de prévention de la corrosion.
La corrosion peut être contrôlée par la peinture, la protection cathodique, la galvanisation ou l'enrubannage (pieux tubulaires) ou une combinaison.
Concept de Protection Cathodique : Cellule Galvanique d'anode, de Cathode et d'électrolyte

La corrosion détériore l'acier, ce qui entraîne beaucoup d'argent pour le remplacer ou le moderniser. La protection cathodique est l'une des options pour contrôler la corrosion.
C'est une technique utilisée pour contrôler la corrosion d'une surface métallique en en faisant la cathode (site moins actif). Une méthode simple de protection relie le métal à protéger à un "métal sacrificiel" plus facilement corrodé ou à servir d'anode (site plus actif).
Si deux métaux différents sont connectés, il y aura une cellule galvanique formée où le matériau plus anodique/moins noble s'oxyde/se corrode. Les matériaux d'anode courants pour la protection cathodique sont l'aluminium, le zinc et le magnésium.

La protection cathodique (CP) augmente la durée de vie et peut être remplacée beaucoup plus facilement que la réapplication de revêtements de protection contre la corrosion. Il peut avoir besoin ou non d'électricité.
Il peut être utilisé en conjonction avec des revêtements anticorrosion pour former un système complet de protection contre la corrosion. Cependant, il ne peut pas être utilisé pour empêcher la corrosion atmosphérique.
La protection cathodique peut protéger des structures telles que des tuyaux, des bases de réservoirs de stockage hors sol, des réservoirs enterrés, des navires, des condenseurs, des tubages de puits, des pieux en acier, des navires et même des structures marines telles que jetée, quai, port, jetée et plates-formes.
Lors de la conception des anodes, les facteurs environnementaux qui doivent être pris en compte sont la durée de vie du système, l'épaisseur du revêtement (le cas échéant), la surface à protéger, la dégradation du revêtement dans le sol, le taux de dégradation du revêtement, la salinité, la résistivité de l'eau de mer, la forte/ eaux mal aérées, débit et température des marées. De plus, le concepteur doit également tenir compte de la capacité électrochimique de l'anode (Ah/kg), de l'écartement de l'anode, de la masse et de la dimension de l'anode.
Le courant anodique total peut être déterminé à partir de la surface de la structure lorsque la densité de courant appropriée a été décidée.
Autres Options de Protection Contre la Corrosion : Peinture, Galvanisation et Ruban Adhésif
Outre la protection cathodique, les autres protections contre la corrosion de l'acier comprennent la peinture, la galvanisation et le ruban adhésif.
La peinture est la méthode d'application de protection contre la corrosion la plus populaire car c'est le moyen le moins cher et le plus simple de prévenir la corrosion. Une peinture épaisse et imperméable peut empêcher les ions de pénétrer dans la surface métallique, réduisant ainsi les risques de formation de rouille. Des additifs tels que les phosphates et les borates sont utilisés comme pigments de protection contre la corrosion pour former des couches de protection au niveau de l'anode. La peinture peut être utilisée en conjonction avec des revêtements de protection cathodique pour former un système complet de protection contre la corrosion. L'époxy, l'uréthane et le polyuréthane sont les peintures anticorrosion passives courantes.
La galvanisation est l'application d'un revêtement de zinc pour protéger l'acier ou le fer afin d'éviter la rouille. Le revêtement de zinc peut être appliqué par galvanoplastie, placage mécanique, shérardisation, fil ou tôle galvanisé en continu, pulvérisation de métal ou galvanisation à chaud générale. Contrairement à la peinture, la galvanisation ne peut pas se faire sur place car elle nécessite de gros équipements. L'exposition à un environnement difficile peut accélérer les dommages au zinc, nécessitant des contrôles d'entretien fréquents. La galvanisation peut être ébréchée et pelée, l'application doit donc être effectuée correctement.
Le ruban adhésif est une autre protection contre la corrosion généralement applicable aux tuyaux. Le ruban adhésif comme la vaseline/cire/graisse peut être utilisé sur de l'eau sèche, humide et submergée, même sans apprêt. Il offre une protection à long terme aux tuyaux, pieux, brides, vannes et a une température de service jusqu'à 230°F (110°C). La couche de ruban de polyéthylène est une autre option de ruban adhésif, mais cela nécessite une couche d'apprêt et plusieurs couches de ruban de polyéthylène.
Courant Imprimé (ICCP) vs Protection Cathodique Galvanique
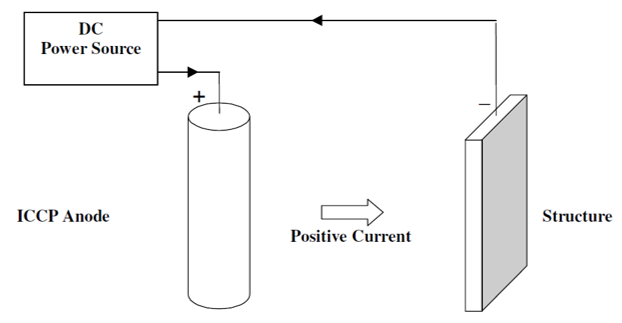
La principale différence entre la protection cathodique à courant imposé (ICCP) et la protection cathodique galvanique est que l'ICCP est connecté à une source d'alimentation externe ou à une alimentation CC afin qu'il puisse entraîner la réaction électrochimique du métal à protéger.
Le transformateur-redresseur connecté à l'alimentation CA peut également être utilisé lorsque le CC n'est pas disponible. Les ICCP sont couramment utilisés dans les structures où les exigences de protection sont élevées. Il peut être ajusté et surveillé en fonction des conditions actuelles.
Puisqu'il utilise une source d'alimentation externe, il a besoin d'un nombre moindre d'anodes par rapport à la protection cathodique galvanique. Il est important de vérifier que toutes les connexions ont l'intégrité de l'isolation pour éviter d'endommager la structure et les autres structures.

D'autre part, les anodes galvaniques sont indépendantes de toute source d'alimentation externe. Il est utilisé pour protéger les zones bien revêtues où les exigences basées sur la résistivité de l'eau ou du sol sont plus faibles. Il peut également être utilisé dans des surfaces plus petites comme le système de mur de palplanches.
Il est plus facile à installer et peut être connecté directement à la structure. Les anodes galvaniques sont autoréglables. Une sélection appropriée des matériaux garantit l'absence de surprotection et d'endommagement du revêtement. Contrairement à ICCP, des connexions incorrectes n'endommageront pas les structures voisines.
Anodes Galvaniques : Magnésium, Aluminium, Zinc

Les 3 principaux types de matériaux d'anode sont l'aluminium (Al), le magnésium (Mg) et le zinc (Zn). Ces matériaux sont plus anodiques/moins nobles donc corrodent et protègent l'acier. Parmi les trois matériaux, le magnésium a le potentiel électro le plus négatif et est mieux utilisé sur les pipelines à terre où la résistivité est plus élevée.
Il est fourni sous forme de ruban ou de type tige et ne convient que pour une utilisation dans les sols et l'eau douce. Le zinc et l'aluminium, en revanche, sont utilisés dans l'eau salée, où la résistivité est généralement plus faible.
Le zinc était autrefois le matériau d'anode traditionnel mais a ensuite été remplacé par l'aluminium car le zinc, avec son activateur de cadmium, est nocif pour l'environnement marin.
De plus, l'aluminium est plus léger, peut protéger de grandes surfaces avec une petite quantité et une tension de commande plus élevée que le zinc. L'aluminium est également le seul matériau qui peut être utilisé dans l'eau saumâtre. Les anodes en aluminium sont couramment utilisées dans les systèmes de murs de palplanches, tandis que les anodes en zinc sont utilisées dans les coques de navires.

Normes pertinentes
Systèmes de Protection Cathodique:
• DNV RP B401 Règles et Normes de Conception de la Protection cathodique
• BS EN 13174 Protection Cathodique des Installations Portuaires
• Autres ressources
• NACE RP 0176
• NACE RP 0386
• NORSOK M503
• BS EN 12473, 12495, 13173
Installation, Mise en Service et Entretien

La connexion typique des anodes à distance sur les palplanches et les palplanches est boulonnée ou soudée. Pour le type soudé, l'installateur ou le client suggère généralement la méthode de soudure humide à utiliser.
La mise en service et la maintenance comprennent:
Enquête de pré-mise en service
Enquête de mise en service
Enquête post-mise en service
Enquête de potentiel annuelle
Inspection visuelle après l'installation
Instruction de rectification

Une enquête de mise en service est menée avant et après l'installation pour vérifier la structure au potentiel de l'électrolyte. Une inspection visuelle après l'installation est effectuée pour vérifier l'état physique des anodes.
Les dimensions des anodes et l'état de corrosion de la structure sont vérifiés pour s'assurer que les anodes ne sont pas sous-protégées ou surprotégées. Sinon, le calcul doit être revu et les rectifications nécessaires doivent être effectuées.
Chez ESC, nous vous aiderons à trouver les bonnes solutions de système de protection contre la corrosion pour votre projet. Obtenez ce dont vous avez besoin pour protéger votre acier dès aujourd'hui !
Envoyez-nous un courriel à escglobal@escpile.com ou contactez nos bureaux près de chez vous!
